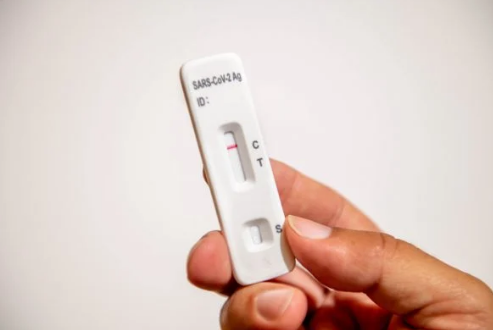
Esta é a segunda vez que a agência se reúne para debater o uso dos produtos. Ministério da Saúde enviou novas informações à agência
Do portal Metrópoles –
A Agência Nacional de Vigilância Sanitária (Anvisa) analisa, mais uma vez, o uso de autotestes para detecção de Covid-19 no Brasil. A deliberação ocorre em reunião extraordinária da Diretoria Colegiada do órgão nesta sexta-feira (28/1).
Esta é a segunda vez que a agência se reúne para debater o uso dos produtos. Na última semana, o órgão adiou a decisão porque o Ministério da Saúde, que solicitou a autorização dos exames, não havia enviado dados suficientes para embasar o pedido.
A liberação dos autoexames será analisada pela relatora do processo na Anvisa, a terceira diretora Cristiane Rose Jourdan Gomes. Para que os produtos sejam aprovados, é necessário formar maioria simples na votação.
Além de Cristiane, os demais diretores também devem formalizar votos: Meiruze Freitas, Rômison Rodrigues Mota e Alex Machado Campos. Antonio Barra Torres, diretor-presidente da Anvisa, não participará da deliberação. De acordo com a agência, o militar precisará tratar de questões pessoais e familiares.
“Se aprovadas, as resoluções são publicadas no Diário Oficial da União no menor tempo possível e entram em vigor conforme texto publicado”, informou a Anvisa sobre a decisão da agência.
Criação de política pública
Ao adiar a autorização dos autotestes na última semana, a Anvisa pediu que o uso dos produtos seja inserido em uma política pública do Sistema Único de Saúde (SUS). Após a solicitação da Anvisa por mais documentos, o Ministério da Saúde enviou nota técnica à agência com novos dados.
No novo documento enviado à agência, o Ministério da Saúde informou que, se autorizado, o uso dos autoexames será incluído no Plano Nacional de Expansão da Testagem para Covid-19 (PNE-Teste). A pasta também ressaltou que os produtos não serão usados como ferramenta de diagnóstico, e sim como plataforma de triagem.
Por isso, após realizar o teste, o paciente com resultado positivo deverá procurar uma unidade de saúde para receber um diagnóstico completo. Além disso, o profissional de saúde deverá registrar o diagnóstico na Rede Nacional de Dados em Saúde do governo federal. No documento, o ministério também detalha como deve ser feita a interpretação e o descarte dos testes, além das exigências às empresas fabricantes.
 Notícias
Notícias








 Entrevistas
Entrevistas Artigos
Artigos Colunas
Colunas Poços de Caldas
Poços de Caldas Agita Poços
Agita Poços Banco de Talentos
Banco de Talentos Classificados
Classificados